Está quase no Natal! Pois é, já passou um período e foi um prazer para mim trabalhar com vocês, ajudaram-me imenso a estudar e evoluir como aluna e espero que tenha acontecido o mesmo com vocês a consultarem este meu blogue! Irei continuar com ele para o próximo período e estou a contar com a vossa companhia! Obrigada por todas as visualização, todos os comentários serão bem-vindos. Irei talvez deixar aqui uns exercícios para vocês praticarem durante as férias. Muitos beijinhos e feliz Natal :)
sábado, 8 de dezembro de 2012
terça-feira, 4 de dezembro de 2012
Constituição da matéria
Agora vamos falar de uma matéria que adoro! Espero que depois de a estudarem e compreenderem gostem tanto dela quanto eu. É uma matéria na minha opinião simplesmente fascinante.
A matéria é contituída por:
A matéria é contituída por:
- átomos
- moléculas
- iões
O que são átomos?
Átomos são:
- Partículas corpusculares, ou seja, extremamente pequenas
- Partículas neutras
- São constituídas por: neutrões - não têm carga elétrica, protões - carga elétrica positiva (encontram-se no núcleo) e eletrões - carga elétrica negativa (encontram-se na nuvem eletrónica)
- Sendo o átomo uma partícula neutra, o número de protões e eletrões é igual (as cargas anulam-se).
TABELAS:
TEORIA CINÉTICO-CORPUSCULAR:
- Toda a matéria é constituída por partículas de tamanho muitíssimo pequeno (corpúsculos)
- Existem espaços vazios entre eles
- + ºC = + agitação/movimentos mais rápidos
- Os corpúsculos estão em constante movimento
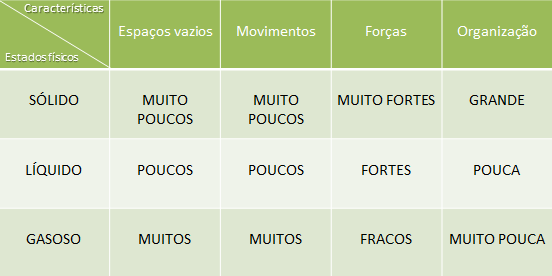
Apresento-vos agora uma tabela que espero que vos ajude a compreender esta teoria, foi inspirada numa tabela que a minha professora me deu e ajudou-me bastante e espero que também vos ajude.
CARACTERÍSTICAS NÃO OBSERVÁVEIS NOS ESTADOS FÍSICOS DA MATÉRIA:
CARACTERÍSTICAS OBSERVÁVEIS NOS ESTADOS FÍSICOS DA MATÉRIA:
MOLÉCULAS:
O que são moléculas?
Moléculas são:
- Conjuntos de átomos ligados entre si
Aqui está um exemplo de como a molécula de água é formada por um conjunto de átomos:
2 átomos de hidrogénio e 1 átomo de oxigénio.
IÕES:
O que são iões?
Iões são:
- Partículas com carga elétrica que derivam de átomos e moléculas.
- Há dois tipos de iões: os que têm carga elétrica positiva: catiões, e os que têm carga elétrica negativa: aniões
- Resultam de um átomo ou de um conjunto de átomos por terem perdido ou ganho cargas negativas - eletrões
- A fórmula dos iões deve indicar o átomo ou átomos que lhe deram origem e deve também indicar a carga do ião.
Se um ião é formado por um só átomo é considerado um ião monoatómico, se é formado por mais de um átomo é considerado um ião poliatómico
LEI DE LAVOISIER:
Lavoisier é considerado o pai da química.
A lei de Lavoisier dita que:
Massa total dos reagentes é igual à massa total dos produtos de reação
ou seja
"Na Natureza nada se cria, nada se perde, tudo se transforma"
E é agora que chegamos aos ACERTOS DAS EQUAÇÕES DE QUÍMICAS. Os acertos das equações químicas baseiam-se nesta lei.
ATENÇÃO: só podes fazer alterações antes das fórmulas químicas como no exemplo.
As Equações químicas dão-nos dois tipos de informações: informação qualitativa (nome do elemento químico) e quantitativa (quantidade do elemento químico)
Deixo-vos aqui um site com diversos exercícios que podem resolver para praticarem exercícios como este e relacionados com o mesmo.
http://nautilus.fis.uc.pt/cec/teses/marta/marta/Jogo/
Há dois tipos de substâncias:
- Elementares
- Compostas
As substâncias elementares são substâncias constituídas por átomos de um único elemento químico.
As substâncias compostas são substâncias constituídas por átomos de diferentes elementos químicos.
 |
| Elementar |
 |
| Composta |
Soluções Básicas, Ácidas e Neutras
 SOLUÇÕES BÁSICAS:
SOLUÇÕES BÁSICAS:As soluções básicas são caracterizadas por:
- Sabor amargo
- São escorregadias ao tacto
- Conduzem a eletricidade
- Alteram a cor de certos corantes vegetais
SOLUÇÕES ÁCIDAS:
As soluções ácidas são caracterizadas por:
- Sabor azedo
- Reagem com metais produzindo hidrogénio
- Conduzem a eletricidade
- Alteram a cor de certos corantes vegetais
SOLUÇÕES NEUTRAS:
São soluções que contêm pH 7
INDICADORES:
Os indicadores são substâncias cuja sua função é contribuírem para a identificação do carácter de uma solução.
Os principais indicadores são a tintura de azul tornesol e fenolftaleína.
TESTE COM O INDICADOR DA TINTURA DE AZUL TORNESOL:
Se a solução for ácida fica vermelha, se for neutra fica azul-arroxeada, se for básica não há alteração da cor
Se a solução for ácida fica vermelha, se for neutra fica azul-arroxeada, se for básica não há alteração da cor
TESTE COM O INDICADOR DE FENOLFTALEÍNA:
Se a solução for básica fica carmim
:
 |
| Solução Básica |
pH:
o pH é a medida utilizada para a classificação do valor da acidez ou basicidade de uma solução. Para isso temos a escala de pH.
Como os indicadores não conseguem medir o VALOR do pH, utilizam-se os seguintes instrumentos:
segunda-feira, 3 de dezembro de 2012
Reações de Precipitação
SOLUBILIDADE:
Uma solução é como sabes uma mistura homogénea de duas ou mais substâncias.
Dentro de uma solução encontra-se um solvente (líquido que dissolve o soluto) e um soluto (substância que se dissolve no solvente).
A solubilidade caracteriza-se pela quantidade máxima de soluto que é possível dissolver numa certa quantidade de solvente a uma determinada temperatura.
As substâncias podem ser então classificadas como solúveis, pouco solúveis e insolúveis.
REAÇÕES DE PRECIPITAÇÃO:
Caracterizam-se pela formação de um precipitado - sólido e pouco solúvel obtido a partir dos reagentes que se encontram dissolvidos.

Uma solução é como sabes uma mistura homogénea de duas ou mais substâncias.
Dentro de uma solução encontra-se um solvente (líquido que dissolve o soluto) e um soluto (substância que se dissolve no solvente).
A solubilidade caracteriza-se pela quantidade máxima de soluto que é possível dissolver numa certa quantidade de solvente a uma determinada temperatura.
As substâncias podem ser então classificadas como solúveis, pouco solúveis e insolúveis.
REAÇÕES DE PRECIPITAÇÃO:
Caracterizam-se pela formação de um precipitado - sólido e pouco solúvel obtido a partir dos reagentes que se encontram dissolvidos.

ATENÇÃO: saltar para os 00:30
Corrosões
 CORROSÃO:
CORROSÃO:Ao processo de deterioração dos materiais dá-se o nome de corrosão.
Das corrosões resultam óxidos devido ao contacto que as substâncias têm com o oxigénio juntamente com a humidade.
.jpg)
Existem porém, metais que ficam naturalmente protegidos da corrosão, nomeadamente:
zinco, estanho e alumínio
Para preservar os materiais e evitar que ocorra a sua corrosão utilizam-se diversas técnicas como:
Pintura; Cobertura com metais que reagem pouco com oxigénio; entre outros (...)
.jpg) |
| Alumínio |
 |
| Estanho |
.jpg) |
| Zinco |
 |
| Tinta |
Esquema de palavras que relata a oxidação do ferro
Subscrever:
Comentários (Atom)





















.jpg)
.jpg)

.jpg)






